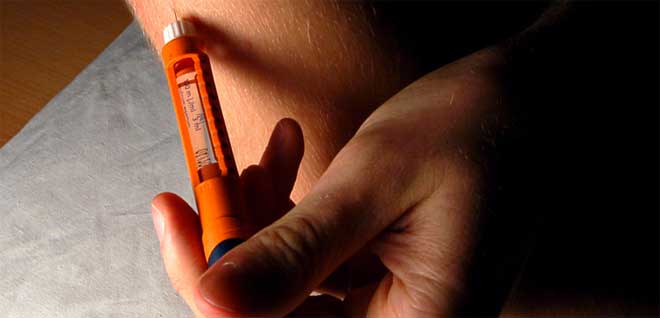
Un páncreas artificial
La incidencia de la diabetes mellitus está creciendo a un ritmo alarmante en todo el mundo. Las consecuencias médicas a largo plazo de la diabetes incluyen:
- complicaciones microvasculares (ceguera, insuficiencia renal y neuropatía)
- macrovasculares (enfermedad cardiovascular, accidente cerebrovascular y enfermedad vascular periférica).
Se ha demostrado que la mejora del control glucémico en los pacientes con diabetes reduce el riesgo del desarrollo y la progresión de algunas de estas complicaciones mayores.
A pesar de la disponibilidad de modalidades de tratamiento cada vez más eficaces, incluyendo los análogos de insulina y controles continuos de glucosa, una proporción sustancial de los pacientes con diabetes no puede lograr un control glucémico adecuado. Esta facultad viene agravada por la búsqueda del equilibrio entre la mejora del control glucémico y un mayor riesgo de hipoglucemia (niveles bajos de glucosa en la sangre), que puede causar convulsiones, coma y muerte.
Muchos expertos creen que la mejor opción terapéutica para el tratamiento de la diabetes es un sistema de páncreas artificial (o de circuito cerrado) que puede imitar la función de las células beta pancreáticas normales restaurando así la homeostasis metabólica normal sin causar hipoglucemia. El diseño de cualquier sistema capaz de lograr este objetivo es complejo y plantea nuevos retos científicos, clínicos y regulatorios.
Como debería de funcionar un páncreas artificial
El término ‘páncreas artificial’ se refiere a un sistema automatizado de control destinado a completar o sustituir el páncreas endocrino alterado funcionalmente en los pacientes con diabetes. Conceptualmente, un páncreas mecánico artificial consta de entradas (por ejemplo, lecturas de glucosa) continuamente alimentadas por un controlador donde un algoritmo matemático aplica un conjunto de reglas para generar una salida (por ejemplo, una bomba de infusión que entrega una cantidad fija de insulina). La información subsiguiente de las entradas podría resultar en ajustes en la salida. Otros fármacos (por ejemplo, el glucagón) pueden estar incluidos en el sistema para contrarrestar los efectos hipoglucemiantes de la insulina o para ralentizar la velocidad de absorción de hidratos de carbono después de una comida (terapias basadas en la incretina, por ejemplo). Los componentes pueden ser externos o implantables y pueden integrar telemetría inalámbrica para mejorar las comunicaciones.
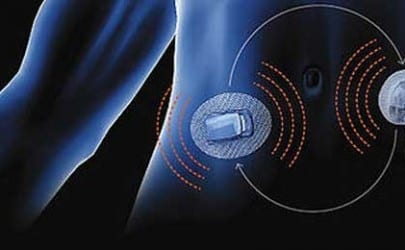
Un páncreas artificial también puede ser enteramente biológico (por ejemplo el transplante de islotes), un híbrido mecánico-biológico, o un sistema semicerrado que implica acciones por el paciente (por ejemplo, la administración al paciente de un bolo de insulina antes de las comidas). Nosotros nos centraremos en este post en el páncreas artificial mecánico.
En EE.UU., en la actualidad, sólo hay un sistema de este tipo que ha sido aprobado por la FDA, (Agencia del Medicamento de Estados Unidos), el Biostator1 (Miles Laboratories, Inc., Elkhart, Indiana). Sin embargo, su gran tamaño y los componentes de muestreo y de administración intravenosa limitan su uso a los ajustes en la clínica.
La tecnología actual
Los dispositivos de medición de glucosa en el líquido interstiticial aprobados usan un tipo de agujas, sensores basados en enzimas que utilizan una reacción de la glucosa oxidasa. Estos dispositivos requieren de calibración utilizando un medidor tradicional de glucosa en sangre, se insertan por vía subcutánea, y deben ser eliminados y reemplazados periódicamente. Las lecturas del sensor se transmiten a un dispositivo como un paginador donde un algoritmo convierte la información a resultados equivalentes a glucosa en sangre. Los resultados actuales y anteriores de glucosa se muestran al usuario para que realice un seguimiento de las concentraciones de glucosa y un seguimiento de la tendencia de la misma. Las limitaciones de estos dispositivos incluyen cambios biológicos y físicos en la interfaz de sensor; por ejemplo, los errores pueden ser causados por una respuesta inflamatoria en el sitio de inserción o por el movimiento mecánico del sensor. También hay retrasos de tiempo de la señal de salida en relación con los cambios en las concentraciones de glucosa en sangre. El rendimiento del sensor es típicamente más pobre en concentraciones peligrosamente bajos de glucosa en la sangre y hay períodos inexplicables cuando las lecturas de los sensores varían significativamente de las lecturas de glucosa en sangre.
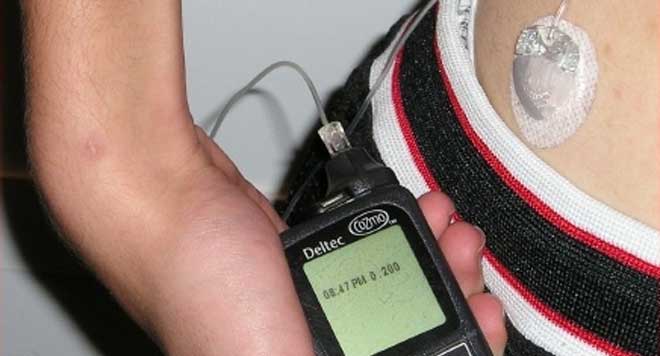
Las bombas de insulina se utilizan a menudo para proporcionar la administración de insulina subcutánea continua. Las bombas extracorpóreas actualmente aprobadas consisten en una jeringa de insulina-cargada que entrega la insulina a través de un catéter. La infusión continua imita la función basal de un páncreas real. Las limitaciones de las bombas de insulina incluyen la absorción lenta y variable de la insulina en la circulación desde el espacio subcutáneo.
Ensayos clínicos
Al menos en teoría, un páncreas artificial podría beneficiar a cualquier paciente con diabetes que no pueda mantener un control glucémico adecuado a pesar del tratamiento médico óptimo.
 Sin embargo, debido a cuestiones de seguridad, el desarrollo inicial de un páncreas artificial podría apuntar a una población de pacientes con la mayor necesidad y potencial para un máximo beneficio (por ejemplo, los pacientes con diabetes tipo 1 frágiles, aquellos que sufran episodios hipoglucémicos frecuentes, o cetoacidosis diabética , o aquellos que no son conscientes de su estado de hipoglucemia).
Sin embargo, debido a cuestiones de seguridad, el desarrollo inicial de un páncreas artificial podría apuntar a una población de pacientes con la mayor necesidad y potencial para un máximo beneficio (por ejemplo, los pacientes con diabetes tipo 1 frágiles, aquellos que sufran episodios hipoglucémicos frecuentes, o cetoacidosis diabética , o aquellos que no son conscientes de su estado de hipoglucemia).
Posteriormente podría ampliarse a:
- Todos los pacientes adultos con diabetes mellitus tipo 1.
- Los niños
- Los pacientes adultos con diabetes tipo 2: a causa de una disfunción progresiva de las células beta, estos pacientes pueden requerir insulina o secretadores de insulina que aumentan el riesgo de hipoglucemia y la inestabilidad metabólica.
- Diabetes gestacional: un páncreas artificial puede alcanzar rápidamente y mantener un excelente control glucémico requerido en pacientes embarazadas con diabetes gestacional que requieren insulina.
- Los receptores de trasplante de células de los islotes: los pacientes con un injerto funcional permanecen libres de hipoglucemia severa, pero pueden requerir insulina exógena. Un páncreas artificial mecánico podría proporcionar suficiente insulina para cubrir las subidas de glucosa en sangre por encima de un valor preestablecido (por ejemplo, 120-140 mg / dl), lo que reduciría el efecto de toxicidad de la glucosa para el injerto y mejoraría el control glucémico y la calidad de vida.
Los ensayos para evaluar un páncreas artificial deben hacerse en un ambiente seguro y controlado, como un Centro de Investigación Clínica.
El desarrollo de nuevas tecnologías
Las nuevas tecnologías podrían tener un impacto en cada elemento del páncreas artificial y a su vez mejorar el funcionamiento general del sistema. La concentración de glucosa en la sangre es una entrada del sistema importante, pero no es la única variable que puede ser utilizada. Es posible medir otras variables de resultado, tales como la actividad física, el consumo de alimentos, la aparición de hipoglucemia, y la función metabólica cerebral.
Se están desarrollando otros sensores para medir la glucosa en sangre indirectamente. Por ejemplo, una tecnología utiliza un láser para crear agujeros microscópicos a través de la capa externa de la piel. Otras tecnologías incluyen la tomografía de coherencia óptica , espectroscopia de impedancia, ácidos borónicos para hacer hidrogeles de poliacrilamida, sensores holográficos y lentes de contacto para medir la glucosa [14,15].
Un número de desarrolladores de productos no invasivos han estado trabajando con sistemas de espectroscopía de reflectancia difusa infrarroja. Si bien se han logrado avances importantes, una relación fundamental entre señal y ruido debe ser optimizada y los investigadores están trabajando para establecer una firma espectral única para la glucosa con respecto a la matriz del tejido .
Una tecnología que está mostrando una promesa significativa se basa en Surface Enhanced Raman Spectroscopy. Parece probable que una versión avanzada de este sensor se podría pasar a través de la piel en el espacio subcutáneo, de una manera similar a la colocación de catéteres basados en bombas de insulina. El sistema basado en nanopartículas puede proporcionar una medida continua y directa de la concentración de glucosa.
Una empresa ha desarrollado un sistema de administración de insulina que está regulada por las concentraciones de glucosa. Este ‘insulina inteligente «es una formulación inyectable una vez al día de insulina. Se compone de un material nanoestructurado (hidrogel) que se autoensambla a partir de dos bloques de construcción biomoleculares: un conjugado de insulina-polímero glicosilada y una molécula de unión de glucosa multivalente. Los investigadores han mostrado resultados prometedores en el estudio de esta tecnología en los animales.
Una empresa aragonesa perteneciente al Grupo Biosalud, denominada Goodday, ha desarrollado una tecnología en la que el glucómetro del diabético se conecta vía wifi con un software inteligente que ha sido desarrollado por la misma empresa, con el asesoramiento de un equipo de endocrinólogos especialistas en Diabetes, de modo que en cuanto el paciente se mide la glucosa en sangre, el dato «viaja» hasta el software, registrando la hora, el nombre del paciente, la glucemia, y a su vez dicho software envía un mensaje al móvil del paciente de buena evolución, de advertencia o incluso un aviso al diabetólogo que lo trata, en el caso de que los valores refieran un peligro para el paciente, para que sea el médico el que se ponga en contacto y aconseje directamente al paciente lo que tiene que hacer. Este sistema estará operativo a primeros de año y ofrecido por Biosalud a cualquier diabético que quiera este servicio en Biosalud en tu casa.
Avances argentinos en el tratamiento de la diabetes

Los médicos de la Universidad Maimónides en Argentina han conseguido que se vuelva a segregar insulina y glucagón, partiendo de células madre propias. Como explica el director de esta investigación, y del Centro de Investigación en Ingeniería de Tejidos y Terapias Celulares (CIITT) de dicha universidad, el Doctor Gustavo Moviglia, por primera vez en el mundo se consigue que el cuerpo vuelva a tener una fuente natural de producción y secreción de insulina y glucagón, que son hormonas complementarias, e igual de necesarias.
Moviglia explica que las pruebas se hicieron con grasa humana, pero sin aplicarlas a individuos. “Después las usamos en animales a los que les habíamos generado un estado parecido a la diabetes. Hasta ahora lo que estamos observando es que suplementan la función”, aclara el director “
“Lo ideal sería que una persona insulino-dependiente , pueda dejar de serlo”- afirma Moviglia-. “Es la meta final que perseguimos. Ojalá lo logremos”
Puede ver este vídeo en el que el Profesor Moviglia habla de esta investigación sobre la diabetes
Moviglia se incorpora a Biosalud como consultor experto
El Profesor Gustavo Moviglia se ha incorporado a Biosalud como consultor experto en Terapia Celular e Ingeniería de Tejidos. Precisamente por este motivo, ha visitado nuestra ciudad y para celebrar sesiones de trabajo en Biosalud como parte del convenio entre ésta y la Universidad Maimónides. Como director de dicho proyecto se ha incorporado a Biosalud Iñigo Sánchez, como experto en asuntos regulatorios y gestión sanitaria, con amplia experiencia a nivel sanitario asistencial y farmacéutico.


